SEMINARIO QUÍMICA ORGÁNICA 26-8-24
EXPOSITOR: Dra. María I. Mangione
TÍTULO: "Concise Total Syntheses of (−)-Crinipellins A and B Enabled by a Controlled Cargill Rearrangement"
DÍA, HORA y LUGAR: Lunes 26 de agosto de 2024, 14:00 h, Aula 18 y virtual.
Modalidad virtual, Link: meet.google.com/hjn-ygro-twf (Plataforma MEET GOOGLE)
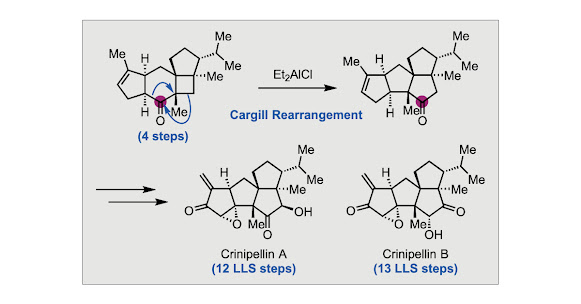
Resumen: En este trabajo se informan las síntesis totales y concisas de los productos naturales diterpenoides (−)-crinipelina A y (−)-crinipelina B. Estos compuestos presentan un esqueleto tetraquinano, tres centros cuaternarios carbonados adyacentes y múltiples grupos oxigenados y funcionales lábiles. En esta secuencia de síntesis pueden destacarse: a) una β-alquilación de Kozikowski convergente para unir dos bloques de construcción que contienen todos los átomos de carbono necesarios, b) una cicloadición fotoquímica intramolecular [2 + 2] para instalar tres centros cuaternarios adyacentes y c) un reordenamiento de Cargill controlado para reorganizar el esqueleto tetracíclico 5–6–4–5 al esqueleto tetraquinano deseado. Estas estratégicas transformaciones permitieron completar las síntesis totales de (−)-crinipelinas A y B en 12 y 13 pasos, respectivamente. Los resultados de cálculos químicos cuánticos revelaron que los reordenamientos de Cargill catalizados por ácido Brønsted probablemente involucran un mecanismo por etapas hacia los productos, mientras que los reordenamientos de Cargill catalizados por reactivos de organoaluminio probablemente implican un camino concertado con desplazamientos de alquilo asincrónicos para formar el producto deseado.
Comentarios
Publicar un comentario